TD for 3enefit!
Willkommen bei TD43
Strukturierte eTD-Erstellung für Medizinprodukte – schnell, zuverlässig und konform.
Wir suchen 1st-in-Medical-Device-Class Kunden!
Medizinproduktakte (MDF, eTD) in 100 Tagen – zum halben Preis? Interessiert?
Über TD43
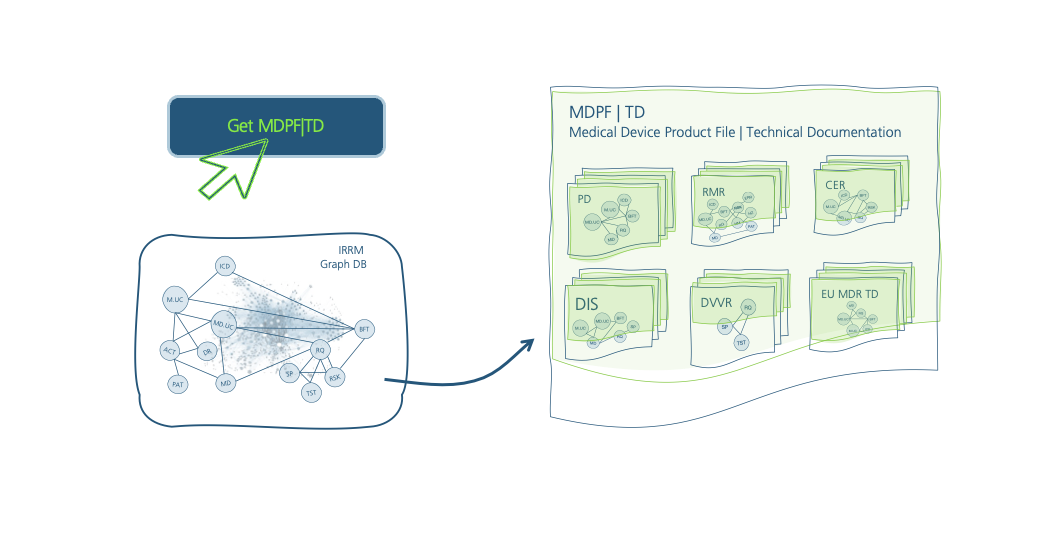
TD43 vereint 20+ Jahre Beratungs-Expertise, ein daraus entwickeltes strukturiertes Datenmodell mit flexibler Graphdatenbanktechnologie und Webplattformtechnologie, um allen Herstellern von Medizinprodukten den regulatorischen Papierkram so weit wie möglich abzunehmen und redundante Arbeiten dauerhaftaus dem System zu entfernen.
TD43 automatisiert die Erstellung konformer elektronischer Technischer Dokumentationen (eTD) für Medizinprodukte – vollständig und konform zu allen internationalen Regulatoren, wie EU MDR, US FDA 510(k).
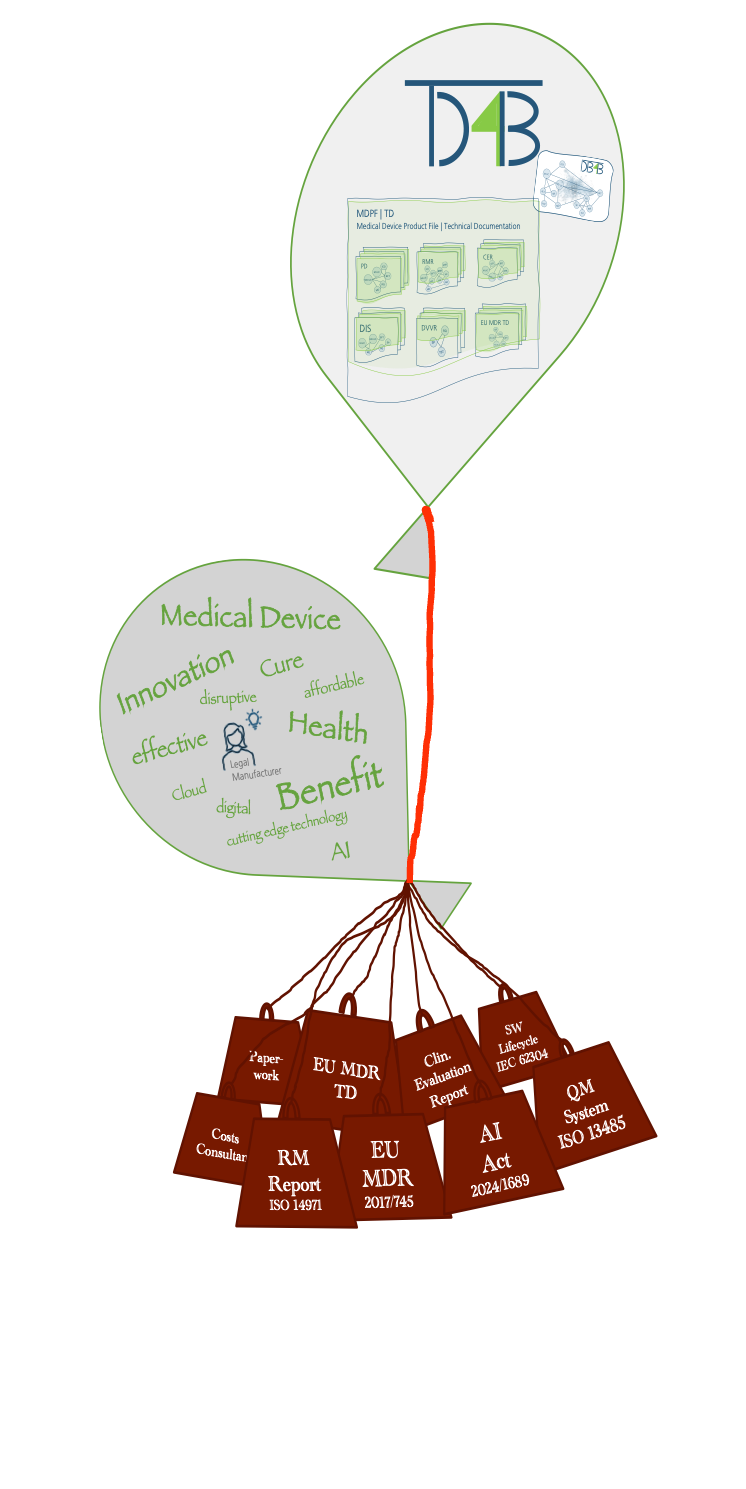
Medizinproduktehersteller, insbesondere Startups sollen unterstützt werden, indem sie eine initiale und umfassende technische Dokumentation mit vollständigem 'Design Input' erhalten.
Diese Medizinprodukteakte nach ISO 13485 inkludiert Zulassungsakten, wie EU MDR TD oder US FDA 510(k) Submission , sowie alle geforderten Unterakten für Risikomanagement (ISO 14971), klinischer Bewertung, oder alle anderen geforderten 'Design Controls' wie Design Output, Design Verification, Design Validation, Design Review und Design Transfer erhalten.
Die Vision ist es zukünftig vollständige Technische Dokumentationen per Knopfdruck für alle Medizinproduktetypen und deren Anwendungsfälle zu ermöglichen.
Der Fokus soll wieder auf die Kernkompetenz der Hersteller übergehen, Design und Development des Produktes und Innovation, für höchsten dreifachem Nutzen für Anwender, Patient und Gesundheistsystem.
Unsere Highlights
Entdecken Sie, was TD43 von anderen unterscheidet:
Innovative Lösungen und maßgeschneiderte Dienstleistungen für die Medizintechnikindustrie.
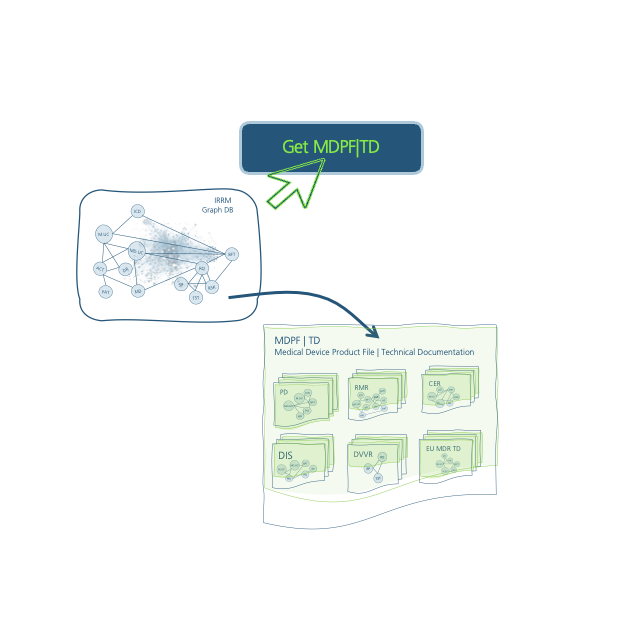
Automatisierte Dokumentation
Alle Design Input Informationen sind struktriert und redundantfrei in einer Datenbank und können auf Knopfdruck in die benötigten Akten und Dokumente (Ansichten, Exportfiles) ausgeleitet werden.

Internationale 'Compliance'
Konformität mit den maßgeblichen globalen Regulierungen und deren Normen und Richtlinien, wie EU MDR, US FD&C, ISO13485, IEC62304, IEC62366, ISO 14971 und alle viele weitere mehr...

Beratungsexpertise
TD43 und alle dahinterliegenden Konzepte resultieren aus einer 20+ jährigen Erfahrung in der Erstellung von technischen Dokumentationen, 10+ Erfahnung in Medizinprodukteberatung und 600+ erfolgreiche Beratungsprojekte. (www.rdh-beratung.de)
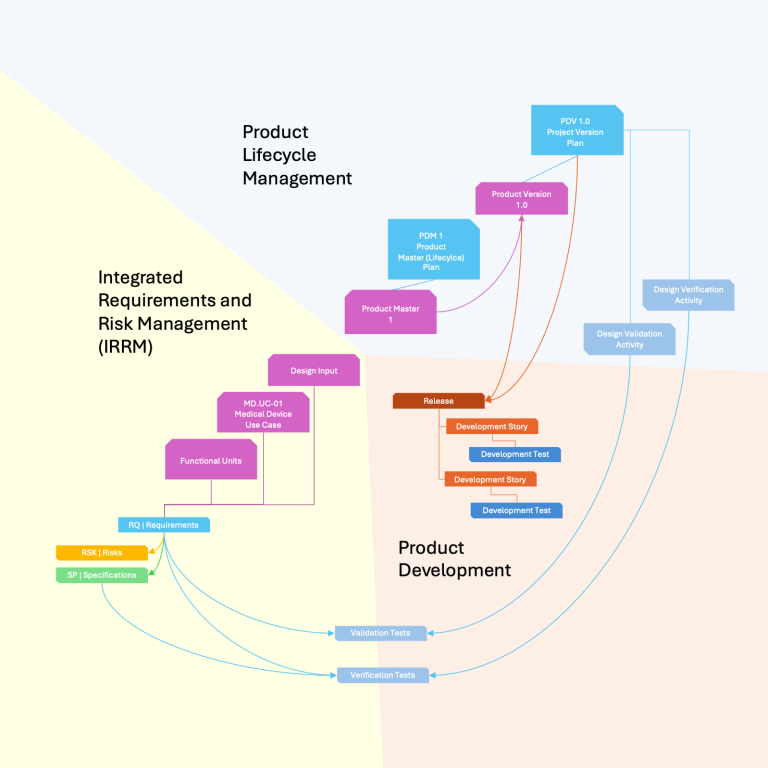
Integriertes Datenmodell
Ein interiertes Datenmodell bedient alle Produktprozesswelten gleichermaßen und umfasst insbesondere Anforderungs- und Risikomanagement in einem integrierten Modell.
20+
Jahre Technische Dokumentation
10+
Jahre Medizinprodukteberatung
600+
Erfolgreiche Projekte
Kontakt
Telefon: +49 163 7623 783
E-Mail: rdh@td43.de
©2025. Alle Rechte vorbehalten.
Wir benötigen Ihre Zustimmung zum Laden der Übersetzungen
Wir nutzen einen Drittanbieter-Service, um den Inhalt der Website zu übersetzen, der möglicherweise Daten über Ihre Aktivitäten sammelt. Bitte überprüfen Sie die Details in der Datenschutzerklärung und akzeptieren Sie den Dienst, um die Übersetzungen zu sehen.
